「萬能細胞」向實用性臨床試驗邁進
2023/04/04
在以臨床研究為主、可分化為所有細胞和組織的「萬能細胞」領域,以實用化為目標的臨床試驗越來越多。繼日本之後,住友製藥(Sumitomo Pharma)2023年內將在美國啟動用iPS細胞治療帕金森病的臨床試驗。世界大型企業諾和諾德(Novo nordisk)將最早於2023年著手進行用胚胎幹細胞(ES細胞)治療帕金森病的臨床試驗。雖然仍存在很多課題,但澳大利亞企業已開始對患者較多的變形性骨關節炎進行最終臨床試驗等,目標是根治疑難病等。
 |
「iPS細胞是源自日本的技術,我們的使命是讓使用這種細胞的再生醫療實現商業化,提供給更多患者」,住友製藥社長野村博表示。住友製藥計劃2023年內在美國啟動初期階段臨床試驗,用iPS細胞治療腦神經細胞發生異常的帕金森病。
帕金森病是運動功能出現異常導致麻木及肌肉僵硬等的疾病。據推算,到2030年,全世界的帕金森病患者人數將達到約1000萬,但目前這種病還無法根治。在日本,2018年京都大學醫院啟動了由醫生主導的臨床試驗,住友製藥的目標是到2024年度在日本國內實現實用化。治療方法是移植由iPS細胞製成的神經細胞,還將在帕金森患者人數較多的美國新設生産基地,為推廣到全世界做準備。住友製藥預計到2032年度再生醫療業務的年銷售額將超過1千億日元,在研究開發上共計投入了超過300億日元的資金。
年內啟動初期階段臨床試驗
諾和諾德利用基於受精卵的ES細胞生成了可産生多巴胺的細胞。計劃最早於2023年內在日美歐啟動初期階段臨床試驗,目標是將這種細胞移植到帕金森患者的腦部進行治療。目前諾和諾德還在利用ES細胞生成可分泌胰島素的細胞,推進用其治療糖尿病的研究。諾和諾德首席執行官(CEO)周賦德(Lars Fruergaard Jrgensen)稱,這種療法「有望從根本上治癒糖尿病」。
 |
| 諾和諾德最早將於2023年內啟動使用ES細胞的臨床試驗 |
安斯泰來(Astellas)製藥也已進入用ES細胞治療有可能導致失明的老年黃斑變性的初期臨床試驗階段。
再生人體組織或器官、使其恢復功能的治療技術統稱為再生醫療。治療手段廣泛,也包括注入基因改造免疫細胞的治療。雖然目前已出現用於重度燒傷患者的培養皮膚等已經獲得批准的産品,但可轉化為所有細胞的ES細胞和iPS細胞尚未得到實用化。
ES細胞方面,2010年美國生物製藥企業傑龍(Geron)在全球首次臨床試驗中為脊髓損傷患者移植了用ES細胞生成的神經。iPS細胞是日本京都大學教授山中伸彌開發的技術,通過在皮膚等的細胞中導入基因來製備,2012年獲得了諾貝爾生理學或醫學獎。理化學研究所2014年對老年黃斑變性患者實施了全球首次臨床研究。大阪大學在心臟病和眼角膜的臨床研究領域走在前面,京都大學在帕金森等的臨床研究方面處於領先地位。
隨著全球臨床研究的不斷積累,在企業的參與下以獲得批准和實現商業化為目標的臨床試驗越來越多。接近實用化的企業是澳大利亞Cynata Therapeutics。該公司以引發疼痛和功能障礙的變形性骨關節炎為對象,使用以iPS細胞製成的幹細胞進行治療,目前正在進行最後階段的臨床試驗。美國有3000萬名骨關節炎患者。
市場規模10年擴大至10倍
據理特諮詢(Arthur D. Little)推測,到2030年,以候選新藥為基礎的「再生醫療與基因治療」的全球市場規模將達到6.8萬億日元,10年時間擴大至約10倍,到2040年將達到12萬億日元。
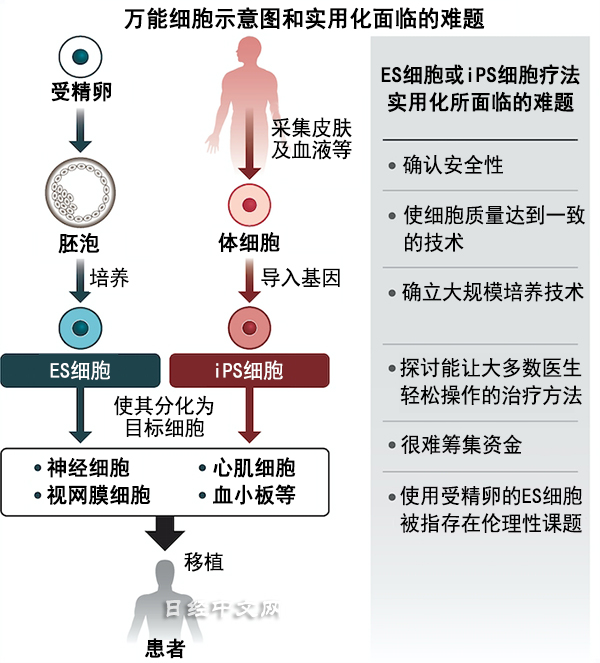
但要實現實用化和普及,還需要解決包括確保安全性等在內的諸多課題。與化學合成藥物不同,活體萬能細胞很難在品質上達到一致。需要高效培養大量高品質的細胞,並掌握安全性確認技術。日本再生醫療學會理事長岡野榮之表示:「重要的是確立讓醫療從業人員輕鬆進行安全管理和注射的方法」,還將考慮制定旨在保證治療品質的醫療設施認定制度。
籌集資金也是一大難題。源自京都大學的初創企業Megakaryon於2022年啟動了利用iPS細胞來治療血小板減少狀態的初期階段臨床試驗。但在籌資方面遇到了困難,「雖然試驗結果良好,但目前已中止臨床試驗」,Megakaryon表示。存在的課題是降低製造成本,Megakaryon正在大力開發可為更多患者輸注的血小板製劑。
也有世界各國普遍採取貨幣緊縮政策的原因,2022年全球對再生醫療領域生物技術企業的投資比2021年減少了約4成。目前,縮減候選新藥的製藥企業越來越多,需要政企學聯合對未來可期的候選新藥採取培育措施。
日本在商業化上落後於人
理特諮詢公司的統計顯示,全世界已啟動臨床試驗的「再生醫療與細胞治療開發産品」共有836種(截止到2022年1月)。美國佔5成,處於領先地位,歐洲不到2成,日本的佔比還不到1成。美國在2020~2021年兩年時間裏增加了6成,呈現出加速趨勢。
在歐美等海外國家,將改造基因的免疫細胞注入癌症患者體內的治療用産品達到總體的7成。而日本則是「癌症以外的再生醫療」産品佔8成,「日本正在醫生的主導下追求(根治疑難病的)理想技術,美國則重視盈利性等,正在致力於治療機制更加明確的領域」,理特諮詢的花村遼指出。兩個國家的傾向不同。
日本一直在iPS細胞的研究方面引領世界,但商業化步伐卻落後於歐美國家。這10年來,日本政府為iPS細胞的實用化投入了1100億日元資金,但這一政策將於3月底結束。目前距離臨床試驗、批准、穩定生産、研發再投資這一週期仍然很遙遠。高品質細胞的穩定生産需要巨大的投資和人才投入。美國國立衛生研究院(NIH)每年向iPS細胞相關領域提供1000億日元的資助。
美歐還在與再生醫療相關的基因治療和基因組編輯方面擁有很多專利。日本的課題是建立相關機制,為政企學相結合的技術開發、商用製造和全球推廣提供支援。
日本經濟新聞(中文版:日經中文網)滿武里奈
版權聲明:日本經濟新聞社版權所有,未經授權不得轉載或部分複製,違者必究。
