新冠口服藥最快年內問世,用藥方便易於量産
2021/09/24
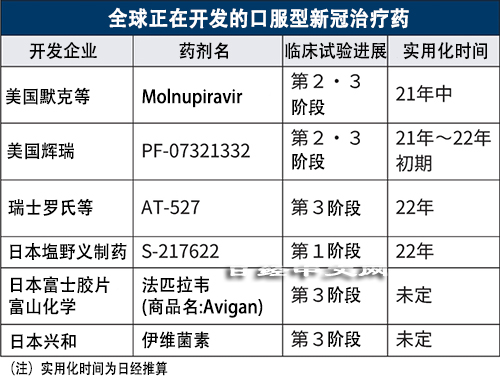
治療新冠病毒的口服藥有望最早在年內問世。美國兩家藥企默克(Merck)和輝瑞(Pfizer)正在包括日本在內的各國推進能用於輕症者的藥劑的最終階段臨床試驗。與點滴注射型的現有新冠治療藥相比除了更容易用藥外,還易於推進量産,更能降低成本。因此,新冠口服藥被期待能推動疫情的全球大流行走向平息。
 |
| 美國藥企默克的抗病毒藥「Molnupiravir」(圖由該公司提供) |
默克正攜手美國新興企業Ridgeback Biotherapeutics開發抗病毒藥「Molnupiravir」。目前正在全球範圍推進臨床試驗,相關數據被認為最早將在10月公開。默克方面還透露了2021年內在美國申請緊急使用許可的計劃。有可能在此之後的1~2個月後在日本申請特例批准。
這款抗病毒藥原本用於流感的治療,但被認為對新冠病毒也同樣有效。美國衛生與社會福利部(HHS)已經與默克簽署了以12億美元採購170萬劑的合同。默克正在推進量産準備工作,力爭到2021年底生産1000萬劑。
 |
美國輝瑞也在研發同樣的抗病毒藥。通過改進2002~2003年面向"非典"(重症急性呼吸症候群、SARS)而開發的藥物,正在開發靜脈注射型和口服型等2種新冠治療藥。相關藥物將並未入院的輕症到中等症狀的患者作為對象。輝瑞透露了2021年10~12月內發佈初步數據的計劃,有望早日實現實用化。
美國的緊急使用許可是在生物恐怖襲擊等非常時期臨時允許未批准藥等使用的制度,本來需要半年至1年的審查時間被縮短至3周左右。與正式批准不同,在安全性和有效性不充分的情況下,也有可能取消批准。
日本也具有特例批准制度,針對美國和英國等存在與日本相同水準藥品審查標準的海外使用的藥品,在非常時期作為特例給予正式批准,允許進口。通常情況下需要半年至近1年的審查時間縮短至2個月左右。
版權聲明:日本經濟新聞社版權所有,未經授權不得轉載或部分複製,違者必究。
HotNews
金融市場
| 日經225指數 | 56941.97 | -697.87 | 02/13 | close |
| 日經亞洲300i | 2681.80 | -15.65 | 02/13 | close |
| 美元/日元 | 152.74 | -0.26 | 02/14 | 04:41 |
| 美元/人民元 | 6.9077 | 0.0080 | 02/13 | 17:40 |
| 道瓊斯指數 | 49610.27 | 158.29 | 02/13 | 14:35 |
| 富時100 | 10446.350 | 43.910 | 02/13 | close |
| 上海綜合 | 4082.0726 | -51.9451 | 02/13 | close |
| 恒生指數 | 26567.12 | -465.42 | 02/13 | close |
| 紐約黃金 | 4923.7 | -147.9 | 02/12 | close |







