日本近期批准15分鐘出結果新冠簡易檢測盒
2020/05/09
關於能進行新型冠狀病毒簡易診斷的「抗原檢測」的檢測試劑盒,日本Miraca控股(HD)的産品有望在日本國內首次獲得實用化。日本厚生勞動省計劃在下周內(5月11起的一週)給予藥事批准。根據現行的PCR檢測體制,從出現症狀到確認呈陽性有時需要約1周時間,但Miraca的試劑盒可在15分鐘內得出結果。雖然在準確度方面低於PCR檢測,但作為前一階段的檢測被認為有效,如果獲得批准,或將推動明顯遲緩的日本的檢測規模擴大。
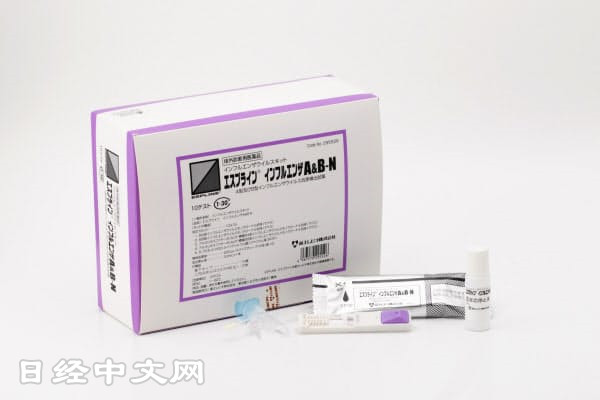 |
| 富士Rebio的流感抗原檢測試劑盒。面向新型冠狀病毒的抗原檢測試劑盒也同樣不需要專用設備,為一次性産品 |
Miraca的子公司富士Rebio(位於東京新宿區)4月27日向日本厚生勞動省申請獲得製造銷售許可。檢測藥的審批在日本通常需要數個月時間,但此次有望大幅縮短。日本首相安倍晉三和日本醫學會也為增加檢測人數而呼籲積極引進抗原檢測。
抗原檢測是通過被用於流感等診斷的方法來檢測被稱為「抗原」的病毒特有的蛋白質。其機制是採集鼻腔內的粘液,滴到試劑盒上,帶有顏色的線將浮現。在醫院等處,醫生可當場在15分鐘左右判斷是否感染。最初,將在日本國內每週生産20萬套,然後根據需求討論擴大生産規模。
在納入公共保險之前,能接受抗原檢測的醫療機構可能僅限於一部分。另外,對於病毒量較少的感染初期的患者,與PCR檢測相比,該檢測的準確度較低。即使通過抗原檢測診斷為未感染,如有疑似症狀,也需要進一步接受PCR檢測等。
目前用於新型冠狀病毒的PCR檢測需要熟悉專用設備和病毒處理的熟練檢測員。難以在中小醫療機構等實施,這成為日本新冠病毒檢測數增長緩慢的原因之一。如果抗原檢測試劑盒得到實用化,有可能有助於檢測體制的加強,這對於經濟重啟等新冠病毒應對舉措的「退出戰略」不可或缺。
除了此次的試劑盒外,富士Rebio還在開發需使用設備的新冠病毒抗原檢測試劑。計劃在6月底之前向日本厚生勞動省申請製造銷售許可。
圍繞新冠病毒的抗原檢測試劑盒,日本中堅化學企業Denka也力爭年內獲得批准,正在加快開發。針對一次性試劑盒,計劃6月之前完成試製品。2021年3月之前構建量産體制,每天最多量産10萬套。
此外,榮研化學也開始討論涉足新冠病毒的抗原檢測。該公司銷售因引發胃腸炎而廣為人知的諾羅病毒等的迅速檢測試劑盒。針對新冠病毒,已推出基因檢測用試劑。該公司社長和田守史表示「關於新型冠狀病毒,在如今的感染高峰過去之後,如何有效使用抗原檢測等方向性並未確定」,同時表示「如果出現必要性被充分認識到的狀態,希望加以討論」。
版權聲明:日本經濟新聞社版權所有,未經授權不得轉載或部分複製,違者必究。
HotNews
金融市場
| 日經225指數 | 56806.41 | -135.56 | 02/16 | close |
| 日經亞洲300i | 2688.31 | 6.51 | 02/16 | 19:16 |
| 美元/日元 | 153.58 | 0.19 | 02/16 | 19:11 |
| 美元/人民元 | 6.9077 | 0.0000 | 02/15 | 23:57 |
| 道瓊斯指數 | 49500.93 | 48.95 | 02/13 | close |
| 富時100 | 10470.100 | 23.750 | 02/16 | 10:01 |
| 上海綜合 | 4082.0726 | -51.9451 | 02/13 | close |
| 恒生指數 | 26705.94 | 138.82 | 02/16 | close |
| 紐約黃金 | 5022.0 | 98.3 | 02/13 | close |







