全球新藥研發在向中國集結
2019/08/21
2018年12月,美國生物企業和英國阿斯利康(AstraZeneca)共同研發的治療糖尿病併發症「腎性貧血」的治療藥——「羅沙司他」在中國獲批,這是該藥物在全球首次獲得批准。羅沙司他目前正在歐美進行臨床試驗。在日本,製藥企業安斯泰來製藥取得聯合研發權,目前仍處於申請生産銷售許可的階段。
中國存在許多未被利用的疾病數據。在中國研發胃癌等亞洲常見的消化器官疾病,還可以輕鬆地出口亞洲。在可以廣泛應用的新藥的研發變得越來越困難的背景下,中國正成為重要的研發基地,並將決定著企業的競爭力。
中國企業在白色家電、智慧手機等領域的市佔率已躍居全球前列,但在醫藥領域尚未顯示出存在感。中國政府提出的産業發展政策「中國製造2025」中提到了生物製藥。目的是積極吸引外資企業投資,提高中國國內的新藥研發實力。
中國每人平均醫療費15年裏增至近10倍
中國擁有超過13億的人口,近年來隨著經濟增長,健康壽命也在延長。據世界衛生組織(WHO)統計,從平均壽命來看,截至2015年,男性達到74.6歲,女性達到77.6歲,以高收入者階層和中産階層為中心,健康意識不斷提高。國民每人平均醫療費2015年達到426美元,增至2000年的近10倍。
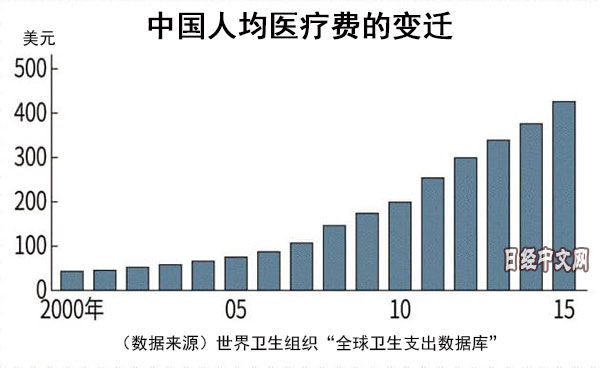 |
市場擴大的原因之一是醫療需求的變化。1990年,感染性疾病佔中國民眾死亡原因的17%,但隨著治療藥物的普及,2015年減少至9.8%。另一方面,高血壓和糖尿病等導致的腦血管疾病和癌症等疾患呈現增加,在疾患構成方面,變得和已開發國家相同。與通過抗菌藥治療的感染性疾病不同,需要手術和高額醫藥費的治療正在推動整體醫療費的上升。
中國市場上流通的藥品的8成被認為是仿製藥,外資企業銷售的藥品也是專利在歐美等國到期的藥品。中國政府針對在國內流通的仿製藥,要求提交再次確認有效性的品質數據,以排除劣質藥品。為了能和已開發國家同步用上新藥,中國還在推進放寬審批限制,致力於提高醫療水準。
版權聲明:日本經濟新聞社版權所有,未經授權不得轉載或部分複製,違者必究。
報道評論
HotNews
金融市場
| 日經225指數 | 56941.97 | -697.87 | 02/13 | close |
| 日經亞洲300i | 2681.80 | -15.65 | 02/13 | close |
| 美元/日元 | 152.73 | -0.27 | 02/14 | 05:50 |
| 美元/人民元 | 6.9077 | 0.0080 | 02/13 | 17:40 |
| 道瓊斯指數 | 49500.93 | 48.95 | 02/13 | close |
| 富時100 | 10446.350 | 43.910 | 02/13 | close |
| 上海綜合 | 4082.0726 | -51.9451 | 02/13 | close |
| 恒生指數 | 26567.12 | -465.42 | 02/13 | close |
| 紐約黃金 | 5022.0 | 98.3 | 02/13 | close |







