全球疫苗開發加速,WHO提出50%有效目標
2020/07/22
全球正在加速開發新冠疫苗。英國藥企阿斯利康(AstraZeneca)7月20日宣佈,通過初期臨床試驗取得了強大的免疫反應。中美企業也將推進自主的疫苗臨床試驗。各公司均將2020年內實現疫苗實用化納入視野,但也存在有效性低的可能性,仍然存在疫苗供給的課題。
「關於向日本供應疫苗,正在與日本政府就1億劑疫苗展開談判」。20日,阿斯利康的首席執行官(CEO)帕斯卡爾·索里奧特對供給體制顯示出自信。原因是在4月啟動的臨床試驗中,發現了一定的預防效果。
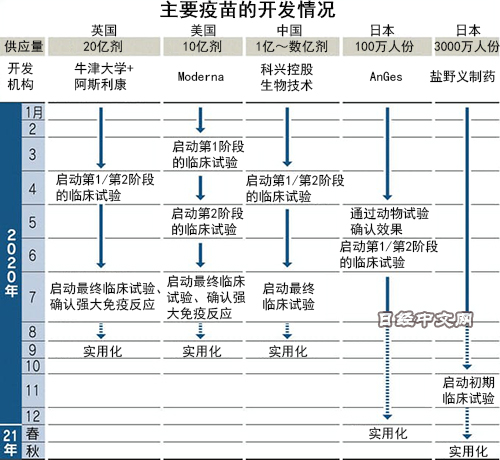 |
世界衛生組織(WHO)的統計顯示,除了阿斯利康的疫苗之外,美國Moderna、德國BioNTech、日本AnGes等的24種候選疫苗的臨床試驗在各國推進。通常的疫苗從啟動開發到結束臨床試驗需要3~5年,但目前很多製藥商將這一時間縮短為半年左右,競爭日益激烈。
此外,各國的支援也是開發速度加快的原因。美國將推進被川普總統命名為「曲率極速行動(Operation Warp Speed)」的官民計劃,這是向疫苗開發和量産提供補貼的機制。受此推動,強生(J&J)將臨床試驗計劃從當初的2021年上半年大幅提前至2020年9月。
在中國,康希諾生物、科興控股生物技術、國藥控股等獲得政府的全面支援,在臨床試驗和供給兩方面加快推進。
課題是疫苗是否實際有效。在疫苗的世界裏,如果有效性為50%,那麼10人中的5人將在接種後仍會發病。70%則是3人,數字越高,越有效果。如果是一般疫苗,有效性達到8成以上,但世衛組織考慮到全球性大流行,針對新冠疫苗,將要求的大致標準定為50%。
已發佈臨床試驗結果的企業並未透露有效性。日本藥企第一三共的常務執行董事籔田雅之表示,「被要求以罕見的速度推進開發,即使是50%也面臨巨大障礙」。
美國國家過敏與傳染病研究所所長安東尼·福奇在美國有線電視新聞網(CNN)的節目中表示,「要遏制新冠病毒,需要70~75%的有效性」,給開發和增産的「趕工」情況澆了冷水。
版權聲明:日本經濟新聞社版權所有,未經授權不得轉載或部分複製,違者必究。
報道評論
HotNews
金融市場
| 日經225指數 | 56363.94 | 2110.26 | 02/09 | close |
| 日經亞洲300i | 2685.39 | 52.87 | 02/09 | close |
| 美元/日元 | 155.68 | -1.20 | 02/10 | 00:40 |
| 美元/人民元 | 6.9216 | -0.0164 | 02/09 | 14:05 |
| 道瓊斯指數 | 50178.20 | 62.53 | 02/09 | 10:35 |
| 富時100 | 10355.740 | -14.010 | 02/09 | 15:30 |
| 上海綜合 | 4123.0897 | 57.5063 | 02/09 | close |
| 恒生指數 | 27027.16 | 467.21 | 02/09 | close |
| 紐約黃金 | 4951.2 | 89.8 | 02/06 | close |







