全球加緊開發新冠藥物,臨床試驗超650項
2020/04/22
在新型冠狀病毒疫情持續擴大的背景下,全球治療藥的開發正在迅速推進。製藥企業通過轉用現有藥物來縮短開發週期,力爭儘早投入市場。此外,還在嘗試採用已康復患者的血液成分的療法,還在挖掘現有的醫療技術和方法。要遏制新冠的勢頭,還需要能夠迅速審查和批准的機制。
新冠治療藥的開發刻不容緩。美國的臨床試驗資料庫顯示,截至4月18日,世界範圍內有650多項新冠的臨床試驗註冊。治療藥、疫苗和再生醫療等各種研究將推進。
在17日的美國股票市場,美國醫藥企業吉利德科學公司(Gilead Sciences)的股價上漲了約10%。這是因為有報告稱,吉利德的伊波拉出血熱候選治療藥「Remdesivir(瑞德西韋)」有助於新冠重症患者的康復。
瑞德西韋作為伊波拉出血熱的治療藥被認為有效性低,開發曾經被中斷。此外,富士底片控股的「法匹拉韋(favipiravir,商品名:Avigan)」也是作為其他疾病的治療藥而被開發。有報告稱二者均具有防止新冠病毒在體內繁殖的效果。
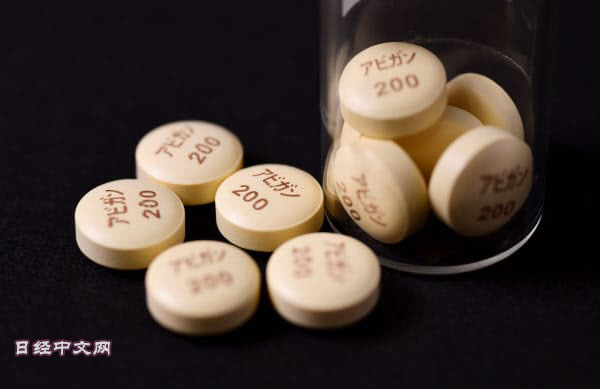 |
| 法匹拉韋(資料圖) |
吉利德宣佈5月即可獲得瑞德西韋的初期臨床試驗數據。如果能確認有效性,將向美國食品藥品監督管理局(FDA)申請批准,最快將在夏季之前在美國的醫療一線使用。
另一方面,法匹拉韋已開始在日美啟動臨床試驗。有猜測認為最快在6月底之前結束臨床試驗,最快年內推向市場。
新冠特有的症狀是重症肺炎。風濕病治療藥被認為具有抑制這種肺炎重症化的效果。瑞士羅氏公司的「雅美羅(Actemra)」和法國賽諾菲等的「Kevzara(sarilumab)」是風濕病新藥。
雅美羅自4月啟動臨床試驗。預計在9月之前結束臨床試驗,力爭今年秋季在美國獲得批准,正在展開行動。Kevzara(sarilumab)預計2021年3月結束臨床試驗,有觀點認為將在之後的1~2個月獲得批准。
版權聲明:日本經濟新聞社版權所有,未經授權不得轉載或部分複製,違者必究。
報道評論
HotNews
金融市場
| 日經225指數 | 57650.54 | 1286.60 | 02/10 | close |
| 日經亞洲300i | 2686.81 | -3.69 | 02/11 | close |
| 美元/日元 | 153.07 | -2.49 | 02/12 | 07:52 |
| 美元/人民元 | / | close | ||
| 道瓊斯指數 | 50121.40 | -66.74 | 02/11 | close |
| 富時100 | 10472.110 | 118.270 | 02/11 | close |
| 上海綜合 | 4131.9850 | 3.6119 | 02/11 | close |
| 恒生指數 | 27266.38 | 83.23 | 02/11 | close |
| 紐約黃金 | 5003.8 | -47.1 | 02/10 | close |







