中國藥企等摸索免疫細胞治療固體癌
2022/02/24
針對在癌症中佔比超過9成的固體癌(Solid Cancer),繼手術、放射線、抗癌劑、免疫藥物之後,又出現了新的治療方法。這種新方法使用改變基因的免疫細胞,改進了在血癌治療中實現實用化的免疫療法。中國的初創企業計劃2023年向美國食品藥品監督管理局(FDA)申請生産銷售許可證,美國企業和日本武田藥品工業也在加緊進行臨床試驗。
 |
全球每年新增癌症患者的人數約兩千萬人,其中約一半人死亡。在每年超過5千萬的總死亡人數中,約佔六分之一。今後,隨著人口的增加和壽命的延長,老年階層將會擴大,預計罹患癌症的人數還會增加。
據美國調查公司BCC Research預測,到2026年全球癌症治療藥物市場規模將達到3137億美元,比2021年擴大77%。其中絕大部分是用於患者人數較多的肺癌及大腸癌等固體癌的藥物。
 |
| 日本BrightPath Biotherapeutics計劃針對骨軟骨瘤和固體癌實施採用CAR-T療法的臨床試驗(圖片由該公司提供) |
癌症目前的主要治療方法是手術、放射線、抗癌劑和免疫藥物。但手術無法切除的轉移性癌症等很難通過放射線和抗癌劑治癒。2010年代開始使用的免疫藥物也很難治療胰臟癌等棘手癌症和晚期癌症。目前,針對白血病等血癌,被稱為CAR-T的療法具有治療效果,對該療法進行改進之後實施的臨床試驗也正接連不斷地展開。
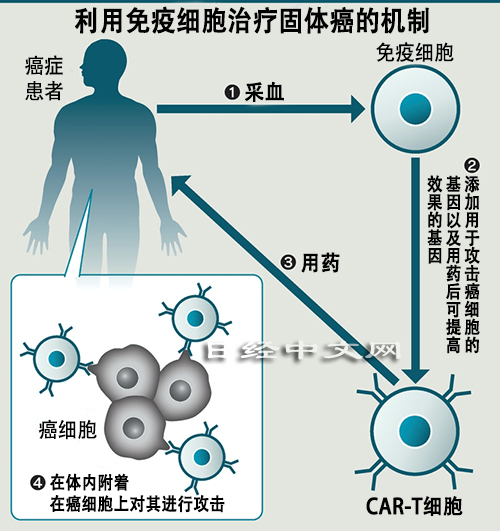
中國醫藥初創企業科濟生物醫藥(CARsgen Therapeutics)利用從患者的血液中提取的免疫細胞製作出了CAR-T細胞。該CAR-T細胞通過向患者的免疫細胞植入可生成用於攻擊癌細胞的CAR蛋白質的基因而製成。該公司還進一步開發出了增強療效的方法。在CAR-T細胞中還追加植入了可生成附著在胃癌和胰臟癌等癌細胞上的蛋白質的基因,從而使CAR-T細胞更容易追蹤和攻擊容易轉移的癌細胞。
科濟生物已在中國完成針對胃癌的第一階段臨床試驗,目前正在計劃實施第二階段臨床試驗。該公司目前還在美國推進第一階段臨床試驗,預定於2023年申請生産銷售許可證。由於該藥被FDA和歐洲藥品管理局(EMA)指定為罕見病藥物,如果臨床試驗能夠證實其效果,將有望在2023年以後上市。
版權聲明:日本經濟新聞社版權所有,未經授權不得轉載或部分複製,違者必究。
報道評論
HotNews
金融市場
| 日經225指數 | 56941.97 | -697.87 | 02/13 | close |
| 日經亞洲300i | 2681.80 | -15.65 | 02/13 | close |
| 美元/日元 | 152.73 | -0.27 | 02/14 | 05:50 |
| 美元/人民元 | 6.9077 | 0.0080 | 02/13 | 17:40 |
| 道瓊斯指數 | 49500.93 | 48.95 | 02/13 | close |
| 富時100 | 10446.350 | 43.910 | 02/13 | close |
| 上海綜合 | 4082.0726 | -51.9451 | 02/13 | close |
| 恒生指數 | 26567.12 | -465.42 | 02/13 | close |
| 紐約黃金 | 5022.0 | 98.3 | 02/13 | close |







